当前,利用二氧化锰(MnO2)构建多功能纳米药物递送体系在癌症治疗及诊断领域得到了极大的发展。MnO2具有低密度、高载药量等优良特性,有利于提高药物递送效率,在肿瘤免疫治疗中发挥重要作用。具体而言,MnO2纳米平台主要发挥以下作用:
一、 制造低氧微环境
MnO2纳米平台能够通过氧化还原反应制造肿瘤病灶周围的低氧微环境,使得癌细胞处于低氧状态,有助于压制与细胞免疫的初级和次要反应,增加癌细胞的免疫逃脱能力。
二、 免疫保护性效应
MnO2纳米平台的特殊结构有利于药物分子的装载和释放。通过将适当的免疫调节剂载入到MnO2纳米平台中,能够唤醒免疫细胞的水平、调节免疫细胞表型及功能,减轻细胞毒性,提高治疗效果,并能够提高癌细胞的免疫反应,达到免疫保护效应的作用。
三、提高化疗效果
MnO2纳米平台对化疗药物和辅料具有优秀的递送效果。将化疗药物载入到H-MnO2纳米平台中,不仅提高了药物的溶解度,也提高了化疗药物的基底稳定性,能够在适量的剂量下实现化疗的效果。
总而言之,利用可生物降解的中空MnO2构建的纳米药物递送平台,不仅可用于肿瘤微环境(TME)的特异性成像和按需药物释放,还可通过调节低氧TME来增强肿瘤治疗,从而产生有利于抗肿瘤免疫反应的综合效应。有研究以中空介孔MnO2为载体,在改善肿瘤乏氧环境的同时,结合光动力治疗(PDT)、化学疗法、基因疗法与免疫疗法“五效合一”联合治疗非小细胞肺癌,取得了不错的效果。
先丰MnO2材料汇总
编号 | 名称 | 应用领域 |
XFI34 | 二氧化锰纳米颗粒 | 电化学、储能 |
XFI33 | 二氧化锰纳米片分散液 | 传感器 |
XFI58 | 中空介孔二氧化锰纳米颗粒 | 药物载体、造影剂 |
XF146 | 超小粒径二氧化锰纳米颗粒 | 模拟酶 |
如您想了解更多MnO2材料的相关资料,可关注“先丰纳米”公众号,将您的要求发送到对话框即可,会有技术专家回复您,您也可以拨打电话025-68256996咨询~
硒是生物和动物必不可少的微量元素,在抗氧化和维持各种代谢过程中的氧化还原稳态方面起到非常重要的作用。随着纳米技术的发展,硒纳米颗粒(selenium nanoparticles, SeNPs)的出现引起了生物医学领域的广泛关注。与普通的单质硒相比,SeNPs在理化性质上有着明显的不同,它可以更好地被机体吸收和利用,较好的发挥机体抗氧化性、抗肿瘤、增强免疫力等功能。本期整理了SeNPs的2个常见应用,一起了解下~
抗菌
近年来,SeNPs在抗菌方面的应用被广泛研究。SeNPs作为广谱抗菌剂具有巨大潜力,对病原细菌、真菌和寄生虫具有重要的抗菌活性。SeNPs直径更小,与细菌细胞膜接触面积更大,可直接破坏细菌的细胞膜,对其造成伤害。如生物材料表面的微生物定植,成为术后感染的一大重要原因,而SeNPs可以抑制细菌生物膜的形成,使其变为浮游形式,增加细菌对抗生素的敏感性。此外,SeNPs可以激活细菌产生活性氧,通过脂质过氧化作用导致细菌膜孔隙率增加,细菌变形塌陷而死亡。进一步研究发现,SeNPs可以下调细菌中相关基因的表达,从而减弱细胞膜功能。
靶向递送
SeNPs经过优化的表面修饰和载体构建后,可以实现对肿瘤细胞的特异性识别和内部传递。SeNPs能够调节细胞内的氧化还原状态,使其在一定程度内处于抗氧化状态。一方面,纳米硒可以促进细胞内一氧化氮合成酶的表达,从而增加单质氧自由基的产生,达到抗肿瘤的作用。另一方面,纳米硒也可以防止细胞内脂质过氧化和DNA损伤等因素的发生,从而起到一定的抗癌作用。SeNPs可以通过抑制细胞周期的调节复制、减少凋亡和增加凋亡、抑制NF-KB、p53 信号通路等方式来抑制肿瘤细胞增殖、迁移和侵袭。多项研究表明,纳米硒能够增强机体的免疫功能,包括自然杀伤细胞的活性、T细胞的活性和白细胞的分泌作用等。通过增强机体免疫力,可以阻止肿瘤细胞的增殖和扩散。
2023年10月,匈牙利科学家卡塔林·卡里科(Katalin Karikó)和美国科学家德鲁·韦斯曼(Drew Weissman)荣膺2023年诺贝尔生理学或医学奖,以表彰他们在核苷碱基修饰方面的发现,他们的发现,从根本上改变了人们对mRNA与免疫系统相互作用的理解,为新冠疫苗的开发贡献了“加速度”。
其实早在新冠疫情期间,mRNA疫苗就已经成为全球关注热点。但是很多人却不知道mRNA疫苗的幕后功臣,甚至可以说是整个机理的关键所在,是将mRNA封装并且安全有效地送进机体细胞的脂质纳米颗粒(Lipid Nanoparticle,LNP)。
为什么这么说呢?
作为一种被寄予厚望的疫苗形式,mRNA疫苗相较于传统的基于生物的疫苗(如减毒活疫苗、灭活疫苗等),工艺简单,合成时间短,安全性高。但是mRNA半衰期短,稳定性差,易被核酸酶降解失去疗效,体内递送效率较低,分子量和负离子性质也为它进入细胞膜屏障带来了巨大阻碍,如何顺利将mRNA完整且高效地递送进细胞成为一个重要议题。
脂质纳米颗粒(LNP)解决了这个问题。
脂质纳米颗粒是由脂质组成的纳米级颗粒,其递送mRNA具有独特优势。首先,LNP为球形颗粒,可将 mRNA 包裹在内,抵御核酸酶的作用;其次,LNP成分与细胞膜类似,易与受体细胞融合,转染效率高,并且不受宿主限制,可以递送不同大小片段的mRNA。目前,LNP已成为递送mRNA最为有效的非病毒载体,并且已经有使用LNP的核酸药物获批,例如,2021年,辉瑞向全球提供了22亿剂mRNA新冠疫苗;同年,Moderna则为全球提供了8.07亿剂mRNA新冠疫苗。
除可以作为mRNA的载体外,由于脂质材料的独特性质和优异的生物相容性,LNPs还适用于纳米药物、疫苗、营养补充剂和不同给药途径的诊断,如口服、局部、肺部和肠外注射。
应广大科研工作者的要求,先丰纳米重磅推出脂质体纳米颗粒,可提供高效的、灵活的、高品质的LNP 中间体合成解决方案,利用已知或新型脂质帮助研究人员还包裹核酸,如mRNA、siRNA、miRNA、pDNA等,解决前端研发难题,提供完善的小试乃至中试工艺方案,
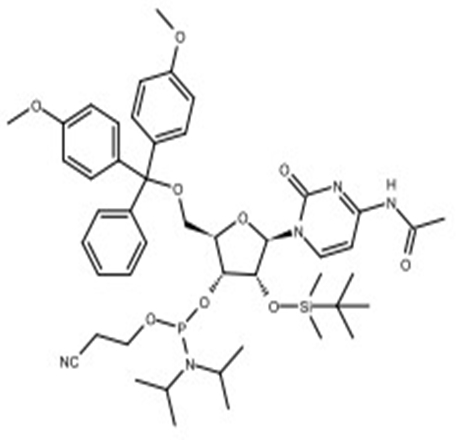
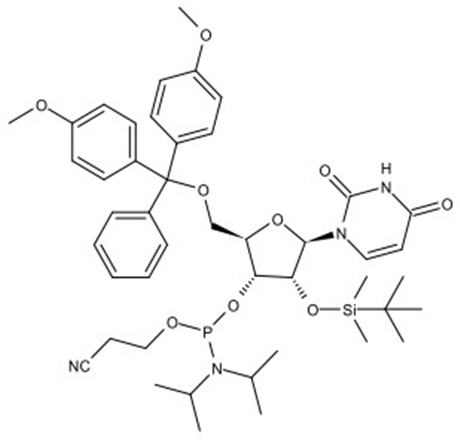
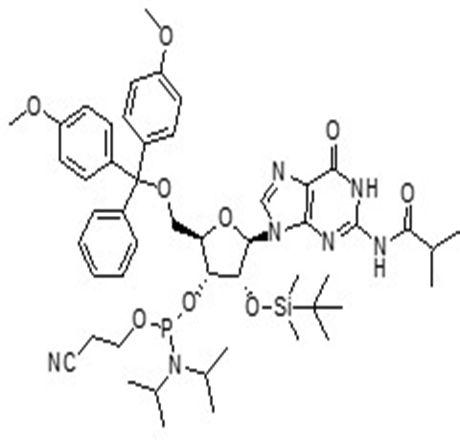
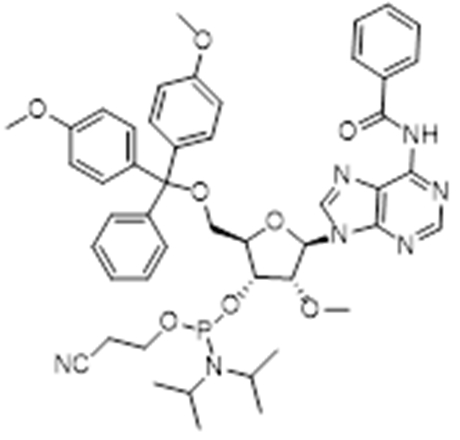
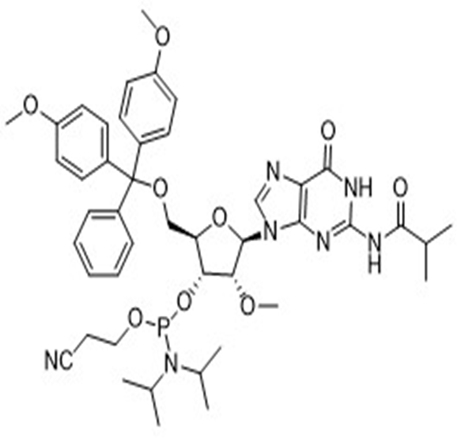
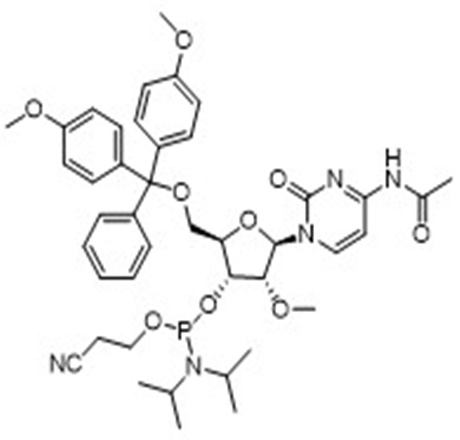
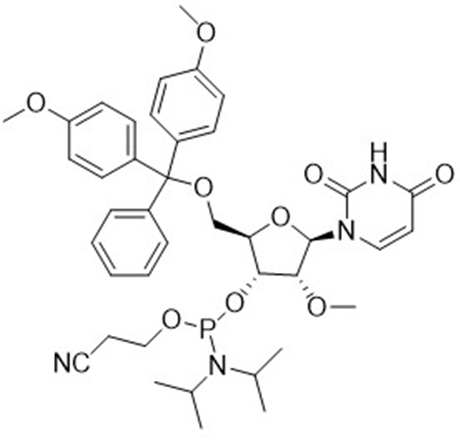
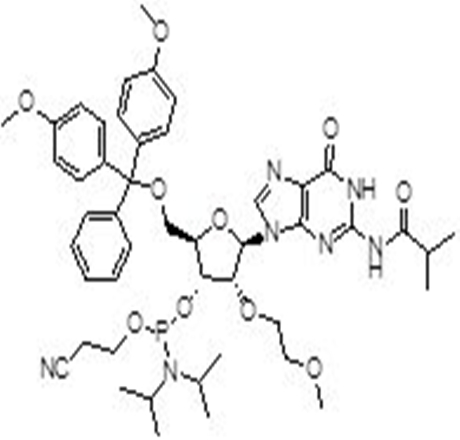
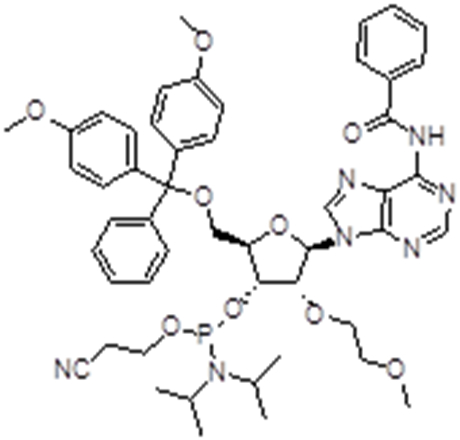
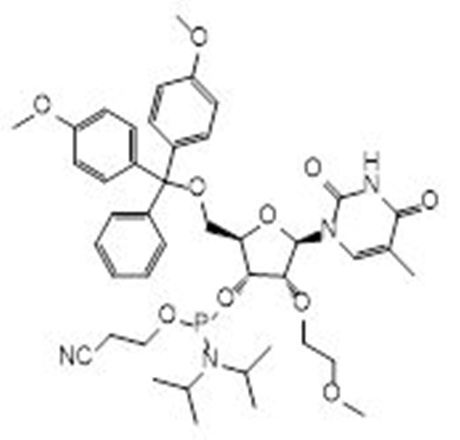
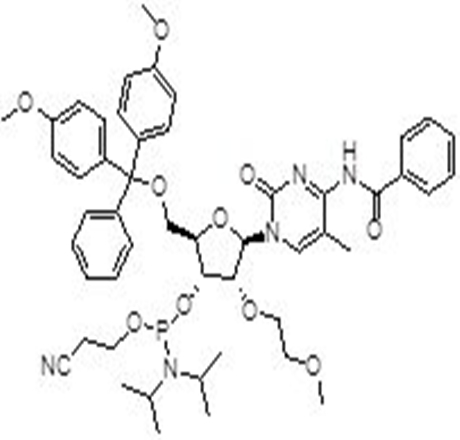
亚磷酰胺单体在化工领域和医药领域都有着广泛的应用。在化工领域,亚磷酰胺单体主要用于制备聚酰胺、聚酰亚胺等高分子材料。在医药领域,特别是在分子生物学和遗传学领域中,亚磷酰胺单体也发挥着重要作用。
如在DNA和RNA的合成中,亚磷酰胺单体是一种重要的原料,它可以通过与胺基反应生成磷酰胺键,将脱氧核糖或核糖与碱基连接起来,从而构建DNA和RNA分子。
其次,亚磷酰胺单体还可以用于基因治疗,如合成基因载体(质粒和病毒载体)等。这些基因载体可以携带治疗基因进入细胞,从而治疗某些遗传性疾病或癌症等疾病。
此外,亚磷酰胺单体还可以用于合成siRNA和miRNA等小分子干扰RNA,用于沉默特定基因的表达,从而治疗某些疾病或研究基因功能等。
近年来,先丰纳米医学领域的客户逐年增多,也对我们提出了希望增加医药研究用材料的期望。为了响应客户的需求,先丰纳米2023年12月重磅推出亚磷酰胺单体材料,主要有RNA系列、OMe系列和MOE系列,欢迎有需求的客户咨询~
聚多巴胺(polydopamine,PDA) 是一种类似于黑色素的物质,具有抗氧化性、光热转换性、粘附性、生物相容性和生物降解等多重特性,得到了科研工作者的广泛关注与研究,自2007年以来已有超过10000篇关于PDA的论文发表。本期带你了解有关聚多巴胺的相关知识~
聚多巴胺(PDA)的特性
高粘附性
2007年美国Messersmith团队在Science杂志发文开创性地报道了PDA对多种材料的黏附特性,此后,PDA涂层作为一种仿生方法,被广泛用于将生物活性物质结合到生物惰性基质上、通过表面修饰增强细胞黏附等,也因此得名“万能胶水”的名号。PDA可以作为中介分子在不同基材表面上连接各类生物活性大分子、从而促进细胞活力。
光热转化
研究表明,PDA在整个紫外、可见和近红外波段内都有高性能的光吸收,且来自光散射的干扰几乎可以忽略不计,因此PDA是一种高效的宽带光热转化材料。摩尔消光系数是评价光热性能的指标之一,能够表示PDA 对于NIR 的吸收能力,PDA 的摩尔消光系数为7.3×108 cm2·mol-1,高出许多PTT 试剂,如硒化铜、碳纳米管和孔雀石绿等。此外,PDA 还具有高达40%的光热转换效率,能够在NIR 照射下(60 min,808 nm,2 W·cm-2)保持结构形态稳定并且光热转换的能量损失很小。
生物相容性
PDA是一种仿生聚合物,具有良好的生物相容性和低毒性。PDA 对A549 和HeLa 的人源细胞系没有急性毒性,MC3T3-E1 和PC12 的鼠源细胞系可以在PDA 涂层表面正常贴附生长,从细胞层面证明了PDA 的安全性。此外,PDA 纳米粒在过氧化氢(H2O2)的作用下会失去紫外吸收,并且伴随有褪色的现象,而机体内还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH)氧化酶广泛存在于吞噬细胞和很多器官中,能够产生H2O2 这种内源性分子,这说明PDA 在体内是可以生物降解的。
聚多巴胺的应用前景
药物递送
PDA 是一种制备简单又可一物多用的载体材料,在构建纳米载体中发挥着关键的桥梁作用,能够将多种功能分子或基团通过PDA 自聚合反应、共价修饰、π-π 堆积和氢键等作用力有机地结合在一起,从而实现“1+1 >2”的协同治疗效果,在药物靶向递送和多模式协同治疗方面具有巨大的发展潜力。
生物电化学传感
PDA具有优良的粘附性,作为修饰材料已成为一种经典的电极修饰方法,被用于电化学传感。聚多巴胺被应用于生物传感的经典例子是在电极表面修饰用PDA包裹的碳纳米管实现了对葡萄糖的检测。该工作中,PDA包覆碳纳米管并将银纳米颗粒嵌入PDA膜中形成纳米复合材料,复合材料与葡萄糖氧化酶一起沉积于玻碳电极表面,当用其检测葡萄糖时,传感器对葡萄糖的酶催化使氧的还原电流降低,从而实现对葡萄糖的检测。
催化
PDA由于具有强粘附性、易于制备和修饰等优点,常被用作酶、金属纳米粒子等催化剂的载体材料。例如,研究人员将葡萄糖氧化酶封装在ZIF 8金属有机框架中,并采用聚多巴胺对其进行包封, 形成微米尺寸的聚集体,极大地提高了葡萄糖氧化酶的重复使用性能。此外,PDA既含有酸性如酚羟基等基团,又含有碱性如伯胺和仲胺等基团,二者分别具有活化其他分子亲核基团或是亲电基团的能力,因此PDA自身也具有催化其他反应的性能。PDA粒子已被证明可以催化CO2与单、双取代的环氧化合物生成碳酸酯。
在聚多巴胺出现以来的16年间,其对表面修饰、生物医药、环境保护、催化、能源等相关领域产生了重要的影响,未来将有越来越多的研究人员加入到聚多巴胺的研究中。
如您想了解更多聚多巴胺的相关资料,可关注“先丰纳米”公众号,将您的要求发送到对话框即可,会有技术专家回复您,您也可以拨打电话025-68256996咨询。
2022年5月5日,ACS Nano报道了氮化硼(BN)纳米片在抗菌领域的研究,发现其对抗生素耐药性(AMR)细菌表现出类似抗生素的活性。BN纳米片具有独立于AMR的抗菌活性,在5种多抗性细菌菌株中表现出强大的抗菌效率,并且在长期使用中没有引发二次耐药性,在哺乳动物中也显示出良好的生物相容性。BN 纳米片独特的Z型环状细菌杀伤机制,可导致细胞分裂中的关键表面蛋白(如FtsP、EnvC、TolB)收缩受损,从而抑制细菌生长。值得注意的是,BN纳米片在绿脓杆菌的肺部感染模型中具有强大的抗菌作用,存活率增加了2倍。该项研究表明,BN纳米片有望成为纳米抗生素用于抑制耐药菌和防止AMR的进化。
文献题目:Antibiotic-Like Activity of Atomic Layer Boron Nitride for Combating Resistant Bacteria
NIR-II荧光染料是指荧光发射位于近红外二区( 1000-1700 nm)的染料。经过多年发展,多种类型的NIR-II荧光染料被成功开发,包括碳纳米管、稀土纳米颗粒、量子点、共轭聚合物和有机小分子等类别。其中共轭聚合物(花菁结构)和有机小分子(D-A-D结构类)NIR-II染料的制备及性能研究已经成为研究热点,尤其在肿瘤成像及荧光手术导航方面取了不错的进展。
类型
花菁素染料。花菁素染料荧光发射峰在近红外一区(700-1000nm),但是发射边可延伸到NIR-II,可用作NIR-II荧光染料。其中最具代表的分子染料是获得FDA批准临床应用的吲哚菁绿ICG,该分子的荧光发射峰在800nm左右,发射边可延伸至NIR-II。
D-A-D类染料。此类型荧光团能隙水平处于可调的NIR-I/II区域,并且其性质能够通过改变给体与受体的结构进行调节。为了进一步降低能带隙,研究人员设计了具有增加电子离域作用的D-A-D结构以制备新型NIR-II荧光分子。
成像应用
北京航空航天大学田捷教授组研制出一种具有高探测灵敏度和高分辨率的可见光和NIR-I/II多光谱成像仪,并首次应用于临床术中肝癌成像和图像引导手术切除。与目前的术前影像学检查(超声,MRI,CT)和术中影像学技术(超声)相比,该研究表明手术中基于ICG的NIR-I/II荧光成像可以检测到没有明显影像学特征的肿瘤病变组织。剖腹手术后,术中NIR-I/II荧光成像能够更为精准的进行患者肿瘤分期并优化治疗方案。
武汉大学肖玉玲等人设计合成了一种基于D-A-D结构的NIR-II小分子染料,通过聚乙二醇改性使得制备的荧光纳米探针具有良好的水分散性和生物相容性。该纳米探针能够被动地富集在肿瘤区域并精确描绘出肿瘤的边界,实现肿瘤的靶向成像和荧光引导的手术切除。
唐本忠课题组设计了一种具有平衡吸收和发射的二合一Janus NIR-II AIE染料,用于图像引导的精密手术。通过在小鼠腹腔内接种大量大小不等的肿瘤模块,建立了小鼠腹腔癌模型。在没有近红外荧光成像的指导下,手术实验中很难精准完全切除肿瘤组织,而在NIR-II荧光成像引导下进行第二轮手术切除,在荧光信号的指导下,微小的肿瘤结节被完全地切除。
尽管目前NIR-II荧光成像等方面取得了一些进展,但在临床中的应用非常有限,仍需更多的努力来解决以下问题,如提高NIR-II纳米探针的特异性、组织穿透性和生物安全性,实现其在癌灶的高效聚集;实现NIR-II纳米探针对于微小转移灶的高灵敏实时示踪等,让我们期待NIR-II荧光探针尽早在临床中得到应用!
Fe3O4纳米粒子在磁靶向药物载体、生物分子分离、磁热疗等生物医学领域有着广泛的应用。但由于Fe3O4的疏水性,使粒子极为容易团聚,且单独的Fe3O4纳米颗粒在空气中不稳定,容易被氧化,难以直接应用。
近年来,有多种类型的材料被用于Fe3O4纳米粒子的表面修饰,包括高分子材料、贵金属、二氧化硅等。其中二氧化硅(SiO2)被认为是在生物医学领域最具前景的磁性纳米粒子修饰材料,主要体现在以下几个方面:
1、包覆的SiO2可以有效地屏蔽磁性纳米微粒的磁性偶极相互作用,减少粒子的团聚;
2、SiO2可以保护磁性纳米微粒不被外界的酸性条件所腐蚀,并提高其生物相容性
3、SiO2稳定性高,可应用于有机、无机溶液,提高磁性微球的分散稳定性,而高分子磁球在有机溶液中易发生溶胀;
4、SiO2表面有大量的硅羟基,易表面修饰及功能化。
磁性二氧化硅纳米粒子的应用
1、靶向药物
SiO2@Fe3O4纳米粒子具有良好的靶向性、生物相容性、功能基团和超顺磁特性等特点,通过外磁场的定位,可在SiO2@Fe3O4材料表面荷载药物并送至病变部位实现靶向给药,特别是用于特定类型癌症的诊断。
近年来SiO2@Fe3O4微球载药系统逐渐朝多功能的纳米颗粒发展,即可以将荧光染料、渗透促进剂、靶向基团、治疗剂、磁共振造影增强剂等连接在纳米粒子的表面或嵌入纳米粒结构中,形成多功能的复合纳米粒子。
2、磁热疗
磁热疗是除了手术、化疗、放射疗法外,另一种治疗癌症的大有前途的方法。磁热疗法治疗肿瘤的机理是利用肿瘤细胞与正常细胞之间不同的热敏感性,当磁流体进人肿瘤组织后,将外部磁场所产生的能量转化成热量进而杀灭肿瘤细胞。
研究人员发现SiO2@Fe3O4粒子被吞噬至肿瘤细胞内,依然保持着单分散的状态,并且在一定的磁场强度下处理1h,仅有10%的肿瘤细胞存活下来,每个存活的肿瘤细胞分裂成2个子细胞,每个子细胞中均含有母细胞中50%的磁性粒子,所以SiO2@Fe3O4修饰过的磁性纳米粒子非常适合细胞的内致热疗法。
3、生物富集与分离
SiO2@Fe3O4纳米粒子在外磁场作用下具有较好的磁响应,可用于生物物质的快速富集与分离。如将磁性二氧化硅直接加入到目标蛋白质溶液中,待目标蛋白质与磁性微粒紧密结合后,利用外部磁场对其进行分离,整个分离过程不需要对混合溶液的pH值、温度、离子强度和介电常数进行调整,从而避免了传统分离过程中蛋白质的损失,分离技术具有快速、高纯、高收率等优点。
硫化铜(Cu2-xS,x=0‒1)纳米颗粒是一种重要的P型半导体,在光学、电学、催化、电池等领域有着广泛的应用前景。让人惊喜的是,在生物医学方面,Cu2-xS具有非常重要的应用价值。由于Cu2-xS纳米颗粒具有局部等离子体共振(LSPR)效应,在近红外光区域呈现较强的光学吸收特性,所以近年来在纳米光热治疗领域如光热疗法(PTT)和光动力疗法(PDT)引起广泛关注。
如有研究发现尺寸为4 ± 0.5 nm的硫化铜(Cu2S)纳米粒子,并在808 nm处的光照射下能够在体内外有效地阻止乙型肝炎病毒组装和防止乙型肝炎病毒感染。明胶辅助共沉淀法合成硫化铜纳米材料在功率为1.0 W/cm2的1064 nm激光照射10 min,几乎能够消融全部癌细胞。
由于Fe3O4的疏水性,使粒子极为容易团聚,且单独的Fe3O4纳米颗粒在空气中不稳定,容易被氧化,难以直接应用。为了改善这种情况,可以在其表面修饰二氧化硅,除此之外,葡聚糖修饰也是一种很好的办法。
葡聚糖与磁性Fe3O4通过范德华力和氨键的作用,使得葡聚糖高分子缠绕在Fe3O4周围,由于葡萄糖良好的亲水性从而可以让修饰后的Fe3O4在溶液中悬浮而不发生沉淀,具有较好的单分散性。此外,高分子葡聚糖上的活性基团经过化学修饰,还可连接抗癌药物以及抗体、活性蛋白和小分子多肽等物质,并配合载体形成磁性靶向载体系统。
普鲁士蓝(Prussian Blue, PB)是一种常见的蓝色染料,大约在1704年,由柏林的一家颜料制造厂意外发现,它也是第一个人工合成的颜料。普鲁士蓝的结构是由Fe(Ⅱ)和Fe(Ⅲ)与氰基(-CN-)相互配位作用构成,具有多孔周期网格框架,所以其也被认为是金属有机框架材料中的一种。普鲁士蓝中的铁物种可以被其他过渡金属(钴,镍,锌,铜,锰等)代替,同时不破坏晶体结构,这样的物质被称作普鲁士蓝类似物(Prussian blue analogues, PBAs)。
普鲁士蓝及其类似物拥有一般MOFs比表面积大、孔隙率高等优点,特别地,普鲁士蓝也是经FDA批准的可用于治疗铊和铯的解毒剂,这充分说明了普鲁士蓝良好的生物安全性,所以PB以及PBAs在生物医药、临床治疗、催化和能源转换等领域都有广阔的应用前景。
【载药】
通过制备中空介孔的PB纳米颗粒或对其表面进行特异性修饰,可以装载大量的药物分子,实现pH响应释放的功能,达到治疗肿瘤的目的。
【解毒】
通过离子交换和吸附作用,PB纳米颗粒能够促进体内放射性铯和铊的排泄,具有解毒效果。
【光热疗】
PB纳米颗粒在808nm激光照射下具有较高的摩尔消光系数,在近红外光的照射下,可以将光能转化为热能,产生局部大于50℃的温度,从而杀死肿瘤细胞。
2022年9月28日,Advanced Functional Materials报道了一种可作为ROS反应开关的甲硫基(SCH3)修饰的介孔二氧化硅(MSNs),并可通过优化合成途径来调整修饰基团的数量、位置和化学结构以及二氧化硅的介孔结构,从而获得理想的最终产物。修饰后的介孔二氧化硅(MSNs)表面的甲硫基在H2O2的存在下被氧化成硫化物,从而影响MSN的疏水/亲水性。合成的MSNs-SCH3的ROS反应行为和纳米颗粒的负载能力使其可以作为一个有效的药物输送平台用于生物医学领域。
羧基中空介孔二氧化硅(球状)
50mg 平均直径:~200 nm;100mg {};50mg {};100mg {};50mg {};100mg {};50mg {};100mg {}
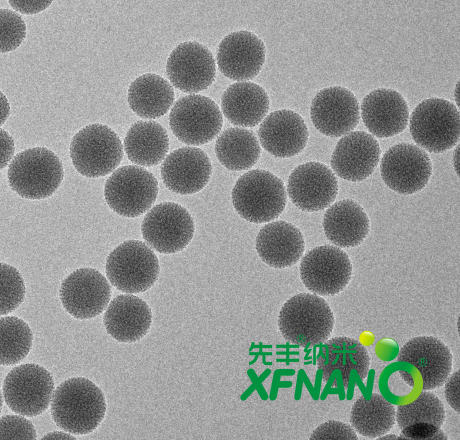
中空介孔二氧化硅(球状)
50mg 直径:~200 nm;100mg {};50mg {};100mg {};50mg {};100mg {};50mg {};100mg {};200mg {};50mg {};100mg {};200mg {};50mg {};100mg {};50mg {};100mg {};25mg {};25mg {};100mg {}
氨基中空介孔二氧化硅(球状)
50mg 平均直径:~200 nm;100mg {};50mg {};100mg {};50mg {};100mg {};50mg {};100mg {};50mg {}
半导体量子点(quantum dots, QDs)是由数百到数千个原子组成的粒径介于1-100 nm的无机纳米粒子。其中IIB-VIA族半导体量子点由于制备简单、光学性质优异而得到广泛的关注,常见的IIB-VIA族半导体量子点主要有CdSe、ZnSe、CdTe、CdS、ZnS等。目前半导体量子点的研究已经成为物理、化学、材料学和生物学等多种学科的交叉点,开辟了半导体材料研究的新领域。
半导体量子点的特性
1. 生物相容性好
经过各种化学修饰之后,量子点可以与生物分子特异性连接;尺寸小,可通过吞噬作用进入细胞;毒性低,对生物体危害小,可进行生物活体标记和检测。
2. 荧光寿命长
可达数十纳秒(20ns-50 ns),而多数生物样本的自发荧光衰减的时间为几纳秒(ns)。这使多数自发荧光背景衰减时,量子点荧光仍然存在,可得无背景干扰的荧光信号。
3. 激发波长范围宽
可以使用小于发射波长的任意波长的激发光激发,因此可用同种激发光同时激发不同尺寸的量子点,发射出不同波长(颜色)的荧光,可用于多组分同时检测。
4. 荧光强度强
半导体量子点比常用的有机荧光染料要强很多,还具有较强的量子点抗光漂白能力(光漂白是指由光激发引起发光物质分解而使荧光强度降低的现象),因此可以对所标记的物质进行长时间的观察,并可毫无困难的进行相关界面的修饰和连接。
半导体量子点的应用
生物学应用
半导体量子点越来越多的作为生物荧光探针用于细胞接受体和体内成像对比,在这些应用中,与传统的有机染料相比较,量子点的高光学稳定性允许长时间的生物过程的跟踪。利用不同颜色发光的量子点可被同一波长的光激发这一性质,还可实现细胞的多色成像。除了成像应用之外,半导体量子点在药物输送、临床诊断、光动力疗法、DNA杂交和RNA分析等领域中也得到了应用。
分析化学应用
量子点的发光与量子点表面的状态的关系非常密切,特定物质与量子点表面发生化学或物理交互左右会影响电子-空穴的结合效率,从而使得量子点可以作为荧光探针应用在光学传感器上。已有的报道表明,半导体量子点可实现对无机金属离子(如Cu2+、Ag+、Fe3+、Zn2+等)实现灵敏的选择性检测,也可以用于气体分子的传感。
氧化石墨烯具有大的比表面积,含有-COOH、-OH、-O-等含氧官能团,具有良好的亲水性和生物相容性,可通过π-π共轭和静电作用于药物分子结合,因此具有被动靶向性从而成为理想的药物载体。近年来,磁性氧化石墨烯(MGO)复合材料的研究取得了很大的进展,研究发现MGO对盐酸多柔比星的负载和释放性能在新型药物载体领域有可观的利用率。此外MGO在磁性环境下可以把负载的药物运输到特定病变部位,在药物传送中具有潜在价值。
研究表明,利用叶酸修饰的MGO可以直接靶向到肿瘤部位起效,增加疗效。研究人员利用PEI修饰的MGO上负载抗肿瘤药物阿霉素,以人乳腺癌MCF-7细胞考察,发现MGO在体外抗肿瘤活性和体外磁靶向性均表现优异。目前MGO已经被应用于生物传感器、生物化学提取和分离、干细胞调节和诱导分化、靶向药物递送和癌症治疗等方面。
2024年2月1日,期刊Nano-Micro Letters在线报道了首个基于紫磷的具有气氛敏感突触行为的光电突触,基于该光电突触首次探索了视觉-嗅觉跨模态感知功能,模拟出具有多感官交互的神经形态视觉。
不同感官的跨模态交互是人脑学习和记忆的重要基础,在器件层面对此进行模拟以发展神经形态跨模态感知是非常必要的,但相关研究却很少报道。该项工作展示了通过将MXene和VP纳米片分散液以不同比例混合后抽滤在带有金电极的滤纸基底上,设计了一个基于MXene/紫磷(VP)范德华异质结的视觉-嗅觉跨模态感知的光电突触。。微观尺度观察发现,MXene/VP异质结网络中复杂的载流子动力学过程导致了持久光电导(PPC)效应,使该器件能够作为光电突触。
由于导电MXene有效促进了光生载流子的分离和输运,VP的光响应度显著提高了7个数量级,达到7.7A·W⁻¹。在紫外线激发下,该光电突触以极低的功耗展示了兴奋性突触后电流(EPSC)、成对脉冲易化(PPF)、短期/长期可塑性(STP/LTP)和“学习经验”行为等多种突触功能。此外,所设计的光电突触在不同的气体环境中表现出不同的突触行为,使其能够模拟视觉和嗅觉信息的相互作用。该项工作证明了VP在光电子领域的巨大潜力,并为虚拟现实和神经机器人等应用提供了一个很有前景的平台。
文中使用的紫磷分散液来自先丰纳米,产品编号XF285-1。
作者反馈:我们的研究所使用的高浓度紫磷烯分散液由江苏先丰纳米材料科技有限公司提供,在该项工作中作为光电突触的光活性层使用。紫磷烯分散液纯度高、分散性好、结晶良好、质量稳定、具有良好的二维形貌,完全满足本工作中光电突触光活性层的应用需要。
在过去的几年里,石墨烯基材料在生物医学领域的应用得到了广泛研究。从最初的作为药物输送的系统开始,如今已经扩展到多种癌症治疗方式的平台的设计之中,包括光热治疗(PTT)、光动力学治疗(PDT)、磁热治疗和声波动力学治疗。其中比较典型的磁性氧化石墨烯(magnetic graphene oxide,mGO)被设计和制造成用于具有多模式响应刺激能力的纳米载体,具有良好的超顺磁性、生物相容性、光热转化性能及癌细胞靶向性,为新型纳米药物载体的合成和应用提供了新思路。本期整理了2篇2024年磁性氧化石墨烯在靶向给药治疗癌症方面的研究进展,一起看下吧~
磁性氧化石墨烯靶向递送阿霉素治疗胶质母细胞瘤
2024年1月13日,International Journal of Biological Macromolecules 报道了磁性氧化石墨烯在靶向给药治疗胶质母细胞瘤方面的进展。研究人员首先制备出壳聚糖修饰的磁性氧化石墨烯(mGOC),然后用胃泌素释放肽(GRP)偶联 mGOC 得到mGOCG。将化疗药物多柔比星(DOX)吸附在 mGOCG 表面,用于双活性/磁性靶向给药。mGOCG 的 DOX 负载为 1.71 mg/mg,并且药物释放对 pH 值敏感,非常有利于药物在内体中的递送。体外研究证实,U87 胶质母细胞瘤细胞对 mGOCG 的内吞作用增强,从而提高了对癌细胞的细胞毒性。与 DOX 和 mGOC/DOX 相比,mGOCG/DOX 的半数最大抑制浓度大大降低。
此外,mGOCG/DOX 还可在磁场(MF)的影响下定位,从而发挥细胞毒性作用。研究人员在 BALB/c 裸鼠的颅内植入 U87 细胞,建立了一个正位脑肿瘤模型,静脉注射不同的样品,通过生物发光成像来研究其在体内的抗肿瘤疗效。与 mGOCG/DOX、mGOC/DOX 或 DOX 组相比,mGOCG/DOX + MF 组显示出最佳的抑制肿瘤生长和延长动物生存时间的效力,表明这种新型 DOX 双靶向给药系统能有效治疗胶质母细胞瘤。
文献名称:Chitosan-coated magnetic graphene oxide for targeted delivery of doxorubicin as a nanomedicine approach to treat glioblastoma
叶酸偶联磁性氧化石墨烯靶向给药治疗肺癌
选择性肿瘤靶向被认为是纳米医学中最先进的方法。靶向治疗可以在癌症治疗中提供更好的治疗效果。与其他聚合物基底相比,二维碳基骨架如氧化石墨烯(GO),有利于多因素表面结构的设计和多种治疗药物的输送,因而成为选择性靶向给药的选择。2024年1月26日,Journal of Drug Delivery Science and Technology探讨了使用叶酸(FA)对磁性氧化石墨烯进行表面修饰,以提高叶酸受体的选择性,从而实现吉非替尼(GF)的主动递送。
石墨烯表面氧基团的存在促进了FA的高负载效率,同时FA 的表面接枝保护了 GF 的过早释放,从而使其可以在目标部位释放,增强治疗效果。体外释放结果表明,GF 在生理环境中释放迅速,12 小时内释放了 80%。同时表面封装的FA提高了抗癌药物的相容性,从而延长了药物在血液循环时间。 A549 细胞毒性实验表明,与纯抗癌剂相比,叶酸(FA)修饰的磁性氧化石墨烯的抑制作用增加了 20 倍。这种多功能化策略还改善了材料的光热效应,FA 接枝后的磁性氧化石墨烯对癌细胞的抑制率进一步提高了 9%。
文献名称:Design and development of folic acid engineered magnetic graphene oxide nanosheets for selective synergistic chemophotothermal inhibition of lung cancer cell
金纳米团簇(Gold nanoclusters,AuNCs)是由几个到几十个金原子组成核心、有机单分子如硫醇类化合物或者蛋白质等作为保护基团组成而成的分子级聚集体。AuNCs粒径一般在2nm左右,介于原子和纳米颗粒之间,最早因为具有一些特殊的光学性质而引起学者的关注。与传统的有机荧光染料和有毒的荧光量子点相比,金纳米簇具有毒性低、荧光性能稳定、生物相容性好、发射波长可调等优点。
近年来的研究发现,AuNCs 具有组分单一、性能稳定、尺寸小以及可肾脏清除的独特优势,已在肿瘤、心脑血管疾病、细菌感染、脑科学、可植入医疗器械等多个领域中得到成功应用。
荧光成像
研究人员制备出Au25 (SR1)n (SR2)18–n型 金纳米簇的靶向淋巴 NIR-II 荧光剂,通过优化阴离子配体类型和进料比例,该荧光剂表现出高效的淋巴结积累以及明亮的 NIR-II 荧光,且比广泛使用的商用淋巴结显像剂 ICG 更加稳定,有利于淋巴结转移诊断和手术指导应用 。此外,还成功地将肝毒性化疗药物(MTX)装载到金纳米簇上,无需繁琐的化学合成即可有效治疗肿瘤转移。载有 MTX 的金纳米簇不仅可以提供与游离 MTX 相当的优异抗肿瘤功效,而且可以显着降低游离药物的肝脏毒性。
抗菌剂
研究人员发现巯基苯硼酸(MBA)修饰的金纳米簇(Au44(MBA)18)对耐万古霉素肠球菌(VRE)等各种耐药菌具有优异的抗菌活性。Au44(MBA)18可首先通过与磷壁酸结合附着在细菌细胞壁上,然后内化并与细菌DNA作用。体外实验表明,Au44(MBA)18能有效杀死多重耐药细菌(超级细菌,尤其是VRE)。体内实验证明,Au44(MBA)18在治疗由超级细菌引起的感染方面具有卓越的效果。此外,Au44(MBA)18还具有极高的生物相容性(无耳毒性),而这正是万古霉素的一大缺陷。与万古霉素相比,Au44(MBA)18可通过多种途径给药,大大提高了其便利性。Au44(MBA)18有望取代万古霉素,成为对抗超级细菌引起的感染的最后一道屏障。
总而言之,金纳米簇作为一种出色的新兴材料,正日益成为一种备受瞩目的生物材料,并有望成为未来的新型药物改变我们的生活。
- 二氧化锰
- 硒纳米颗粒
- 脂质体纳米颗粒
- 亚磷酰胺单体
- 聚多巴胺
- 氮化硼
- 近红外二区荧光染料
- 磁性二氧化硅
- 硫化铜
- 四氧化三铁
- 普鲁士蓝
- 二氧化硅
- 半导体量子点
- 石墨烯
- 紫磷
- 金纳米簇