产品名称
中文名称:羧基化脂质体纳米粒子
英文名称:Carboxylated Liposome Nanoparticles
产品概述
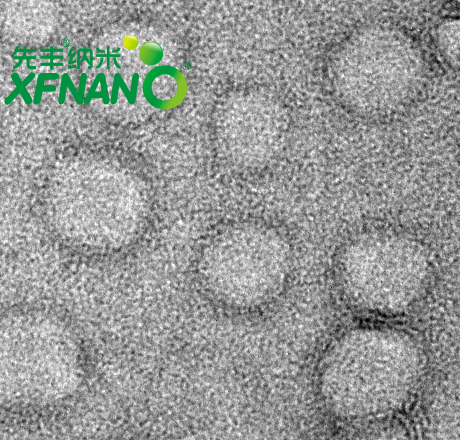
羧基化的脂质体纳米粒主要由脂质分子组成,这些脂质分子在水中自发形成双分子层的囊泡结构。通过引入羧基基团,可以在脂质体的表面或内部形成特定的化学修饰。这种修饰通常通过化学反应实现,如使用含有羧基的化合物与脂质体反应,从而在脂质体上引入羧基。这种化学修饰赋予了脂质体纳米粒新的特性和功能,使其在药物传递、生物成像、基因治疗、化妆品、护肤品等领域具有广泛的应用前景。
技术参数
形态:半透明乳液
溶剂:水
成分:卵磷脂、胆固醇、羧基聚乙二醇
产品特点
增强药物的稳定性:羧基修饰可以提高脂质体纳米粒对药物的包封效率和稳定性,防止药物在递送过程中泄漏或降解。
提高靶向性:羧基化脂质体纳米粒可以与其他分子(如抗体、多肽等)偶联,形成具有主动靶向功能的药物递送系统,将药物精准地输送到病变部位。
改善溶解度:羧基修饰可以改善脂质体纳米粒对药物的溶解度,使其能够包封更多种类的药物,包括亲水性和疏水性药物。
良好的生物相容性:脂质体纳米粒本身具有良好的生物相容性,羧基修饰进一步增强了其生物安全性和生物利用度。
应用
药物传递:作为药物载体,羧基化脂质体纳米粒可以将药物精准地输送到病变部位,提高治疗效果并降低副作用。
生物成像:利用脂质体纳米粒的荧光性质或磁性性质,可以构建高灵敏度的生物成像探针,用于细胞成像、组织成像和肿瘤成像等。
基因治疗:羧基化脂质体纳米粒可以作为基因载体,将外源基因安全有效地导入细胞内,实现基因治疗的目的。
其他信息
如您想了解更多产品详情,可拨打电话400-025-3200,您也可以发送邮件到sale@xfnano.com咨询

mRNA疫苗的幕后功臣-脂质体纳米颗粒
2023年10月,匈牙利科学家卡塔林·卡里科(Katalin Karikó)和美国科学家德鲁·韦斯曼(Drew Weissman)荣膺2023年诺贝尔生理学或医学奖,以表彰他们在核苷碱基修饰方面的发现,他们的发现,从根本上改变了人们对mRNA与免疫系统相互作用的理解,为新冠疫苗的开发贡献了“加速度”。
其实早在新冠疫情期间,mRNA疫苗就已经成为全球关注热点。但是很多人却不知道mRNA疫苗的幕后功臣,甚至可以说是整个机理的关键所在,是将mRNA封装并且安全有效地送进机体细胞的脂质纳米颗粒(Lipid Nanoparticle,LNP)。
为什么这么说呢?
作为一种被寄予厚望的疫苗形式,mRNA疫苗相较于传统的基于生物的疫苗(如减毒活疫苗、灭活疫苗等),工艺简单,合成时间短,安全性高。但是mRNA半衰期短,稳定性差,易被核酸酶降解失去疗效,体内递送效率较低,分子量和负离子性质也为它进入细胞膜屏障带来了巨大阻碍,如何顺利将mRNA完整且高效地递送进细胞成为一个重要议题。
脂质纳米颗粒(LNP)解决了这个问题。
脂质纳米颗粒是由脂质组成的纳米级颗粒,其递送mRNA具有独特优势。首先,LNP为球形颗粒,可将 mRNA 包裹在内,抵御核酸酶的作用;其次,LNP成分与细胞膜类似,易与受体细胞融合,转染效率高,并且不受宿主限制,可以递送不同大小片段的mRNA。目前,LNP已成为递送mRNA最为有效的非病毒载体,并且已经有使用LNP的核酸药物获批,例如,2021年,辉瑞向全球提供了22亿剂mRNA新冠疫苗;同年,Moderna则为全球提供了8.07亿剂mRNA新冠疫苗。
除可以作为mRNA的载体外,由于脂质材料的独特性质和优异的生物相容性,LNPs还适用于纳米药物、疫苗、营养补充剂和不同给药途径的诊断,如口服、局部、肺部和肠外注射。
应广大科研工作者的要求,先丰纳米重磅推出脂质体纳米颗粒,可提供高效的、灵活的、高品质的LNP 中间体合成解决方案,利用已知或新型脂质帮助研究人员还包裹核酸,如mRNA、siRNA、miRNA、pDNA等,解决前端研发难题,提供完善的小试乃至中试工艺方案,
江浙沪皖用户邮费为10元,其他地区用户邮费为20, 国际运费请咨询sales@xfnano.com。购买满 500.0 元免运费。如果库存显示为0, 请电话或邮件和销售确认,免费热线电话:400 025 3200邮件:sale@xfnano.com 感谢您的支持!